減肥食品不只是種類多,問題也是超級多。市售的減肥食品百百種,到底哪種有效,哪種沒效?到底有沒有科學根據?延續上一篇介紹抑制吸收類減肥食品的文章,這一篇會接著向介紹減重食品最常見的類型 – 促進新陳代謝!不管在之前做市場調查還是這次回顧的成分裡,可以說大部分的減重食品都會用上這類的成份,至於效果如何呢?
為了解答這個問題,團隊的醫師和營養師總共整理了 16 種減重成分,並且回顧了 90 篇文獻!上一篇文章主要是講抑制吸收類的成分,這篇文章則會主打促進新陳代謝類的成分,並且把其他機制的產品一次講完!這篇文章很長,先說明使用及閱讀方式:
- 你不太可能看完整篇的。可以直接點選你有興趣的成分進去看。
- 文章上半段是在講目前證據上傾向沒什麼效果的成分
- 文章下半段是在講目前證據上比較可能有效的成分
- 每個成分都會附上相關的研究的摘要
- 你可以根據自己想選用的產品成分,去判斷可不可能有效果,但要注意劑量問題,不宜過多,但過少可能也沒效。另外千萬不要忘記,體重是你生活習慣的總和,絕對不會是你吃某種產品就可以瘦、而且做到持久瘦喔!
在這篇文章開始前,請大家先複習一下減肥產品的四大方向:
- 抑制食慾
- 抑制消化吸收
- 促進新陳代謝
- 減少慢性發炎
今天的內容的內容,將介紹除了抑制吸收這類產品「之外」的各種成分喔!
快速檢索減肥食品成分中:
傾向被認為無效或無結論的成份
鈣質辣椒素和辣椒素類物質褐藻素仙人掌覆盆子酮維生素D
傾向被認為可能有效的成份
非洲芒果苦橙咖啡因肉鹼鉻共軛亞油酸藤黃果綠咖啡豆萃取物綠茶與綠茶萃取物益生菌
減肥食品成分中傾向被認為無效或無結論的成份
這類成分我們不會用太多篇幅介紹,只要知道它們對減重無效,或相關研究不足以給出確定的答案就好。
鈣質
就是那個貯存在骨骼與牙齒的礦物質「鈣」,舉凡血管收縮與擴張、肌肉功能運作、神經傳遞、細胞內訊息,還有荷爾蒙分泌等生理作用都需要鈣的參與。有好幾個研究發現鈣補充與較低體重或較少體重增加有關( Ref. 2, 3, 4, 5 ,6 )。
鈣有助於減重的可能機制有兩個,第一,高鈣攝取可能因副甲狀腺素與活化維生素D 的關係,使得脂肪細胞裡的鈣濃度減少。接著,細胞內鈣濃度降低很可能會增加細胞內的脂質分解作用,以及阻止脂肪的堆積( Ref. 4 )。第二,鈣質可能和飲食的油脂在消化道中結合,因而阻礙脂質的吸收( Ref. 5, 7, 8 )。
減重效果:對體重、減重或預防體重增加沒有效果
安全性
成人每天攝取 1,000-1,200 毫克是安全的,但參與者回報的副作用包含便秘、腎結石。還有,成人攝取劑量高到 2,000-2,500 毫克可能干擾鋅與鐵的吸收。
辣椒素和辣椒素類物質

辣椒素類物質是主要讓辣椒有辛辣刺鼻風味的成分,其中含量最多且研究最多的是辣椒素( Ref. 9 )。一般認為辣椒素能增加能量消耗和脂質氧化,且能減少餐後胰島素反應、增加飽足感、減少食慾與能量攝取,因而可能有減重的作用。
減重效果:可能減少能量攝取,但對體重沒有影響
安全性
連續 4 週,每天攝取 33 毫克,或連續 12 週,每天攝取 4 毫克,可能會有安全上的問題。研究參與者曾出現以下副作用腸胃不適、胰島素增加、減少 HDL 的濃度等。 ▴ Back
褐藻素( Fucoxanthin )
褐藻素是一種常見於褐色的海藻和其他藻類的類胡蘿蔔素。體外與動物研究發現褐藻素可能有助於減重的機制是增加休息時能量的消耗與脂肪酸的氧化作用,以及抑制脂肪細胞的分化與脂質的堆積( Ref. 10, 11 )。
減重效果:研究太少不足以給出確切的結論
安全性
試驗中,連續 16 週,每天 2.4 毫克的劑量,沒有安全上的疑慮。研究中,受試者沒有回報任何副作用。
仙人掌( Hoodia )
仙人掌(學名: Hoodia gordonii )是一種生長在南非卡拉哈裡沙漠裡的多肉植物。當地人在長時間狩獵時,就會吃仙人掌來抑制食慾,後來就因為這典故,以及一些動物研究的結果指出仙人掌能減少食物攝取的關係( Ref. 12 ), 2000 年代添加仙人掌萃取物的減重產品曾在美國流行過,之後台灣也曾經流行了一陣子。
減重效果:從一篇研究的結果顯示對能量攝取或體重沒有效果
安全性
有些安全疑慮的報告,增加心率與血壓。參與者回報的副作用有頭痛、頭暈、噁心與嘔吐。 ▴ Back
覆盆子酮( Raspberry ketone )

覆盆子酮是紅色覆盆子(學名: Rubus idaeus )主要的芳香化合物,可當做調味料使用( Ref. 13 )。體外和動物研究支持覆盆子酮很可能增加脂肪酸的燃燒來幫助減重,並且能抑制脂肪堆積及抑制胰臟脂肪分解酵素的活性( Ref. 14 )。
減重效果:研究太少不足以給出確切的結論
安全性
在一個 8 週的試驗裡,並沒有出現安全性的問題,參與者並沒有回報任何的副作用。 ▴ Back
維生素D
維生素D 是脂溶性的維生素,僅出現在一部分的食物中,例如魚、起司、蛋黃、菇類等。維生素D 跟減重會有關係是因為有觀察研究發現較低維生素D 與較多的體重有關係,此外,肥胖者血中維生素D 的濃度很常處在接近邊緣或缺乏的狀態( Ref. 15 )。
減重效果:無效
安全性
在正常攝取下沒有安全的疑慮(請參考維生素D 的文章);但攝取過多會有毒性,成人耐受的上限是 4,000 IU/ 天。可能的副作用有厭食、體重減輕、多尿、心律不整、血鈣增加可能導致血管與組織鈣化。 ▴ Back
減肥食品成分中傾向被認為可能有效的成份
以下的減肥食品成分,在相關的實驗中被認為可能有效。但是有效的程度,以及實際的用量,這兩件事情大家都是要考慮在內的,不要看到這成分有效,就立刻衝去買喔!
非洲芒果( African mango )
非洲芒果( African mango ,學名 Irvingia gabonensis )是一種原生於西非與中非的樹種。從體外試驗發現非洲芒果的種仁萃取物有抑制脂肪形成的作用,因此被認為對減重有幫助。市面上有一支專利萃取的非洲芒果原料,研究發現它具有降低瘦體素的作用。什麼是瘦體素呢?它是一種和體重及體脂有正向關係的荷爾蒙,也就是說體內瘦體素濃度越高,體重與體脂肪就可能會比較多。此外,研究也發現該非洲芒果萃取物也能降低總膽固醇與 LDL 的濃度( Ref. 16 )。
減重效果:對體重與腰圍可能有些減少的作用
研究證據
已經有研究調查非洲芒果在減重上的效果,不過相關人體試驗的數量有限。有篇在喀麥隆進行,隨機將 102 位體重過重或肥胖的人分配的非洲芒果萃取物組( 150 毫克/次)或安慰劑組,在中餐與晚餐前 30 到 60 分鐘內吃試驗膠囊,試驗進行時間是 10 週。試驗結束後,非洲芒果組的體重、體脂與腰圍顯著低於安慰劑組。
2013 年有篇系統回顧( Ref. 17 ),除了上述的研究也包含另外兩篇研究,結論是非洲芒果萃取物在減輕體重與腰圍有達統計顯著的意義。不過作者強調該研究回顧到的文獻用了不同的研究方法,且樣本數太小、試驗時間短,還有使用劑量不同的關係( 300 ~ 3,150 毫克),都是同一個作者進行的研究。因此需要進行更大規模且以不同人群為對象的研究才能確定非洲芒果的減重功效。
安全性
非洲芒果萃取物似乎有良好的耐受性。讓老鼠每天吃 2,500 毫克/公斤的劑量並沒有出現任何副作用,不過在人類身上還沒經過嚴格的研究。
大部分研究報告提到的副作用都很輕微,症狀包含頭痛、難以入眠、脹氣。不過,非洲芒果被認為和患有慢性腎臟疾病的腎衰竭有關係( Ref. 18 ),因此為安全起見患有腎病的人建議避免食用含有非洲芒果的產品。 ▴ Back
苦橙( Bitter Orange )

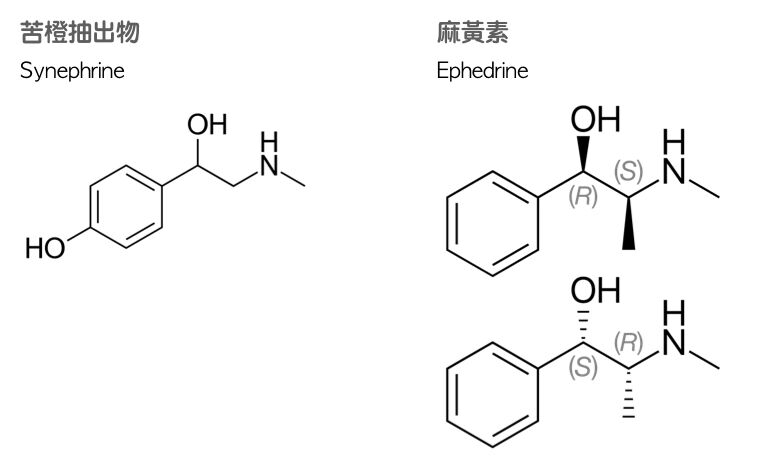
苦橙,學名是 Citrus aurantium ,果實含有豐富的 synephrine 和其他生物鹼,這些成分可能發揮 α-腎上腺素促效劑,會有如此作用的原因在於 synephrine 能模仿腎上腺素與正腎上腺素的作用。不過,苦橙和 synephrine 是否能像真的腎上腺素與正腎上腺素那樣對心血管與中樞神經系統作用呢?目前還不是很確定( Ref. 19, 20, 21, 22 )。
有些研究支持苦橙能增加能量的消耗與脂質分解,並有稍微抑制食慾的作用( Ref. 19, 21 )。自從 2004 年禁止於膳食補充品添加麻黃生物鹼之後,廠商開始用苦橙來取代。雖然 synephrine 的結構某種程度和麻黃素有點類似,但藥理的性質其實不太一樣。
減重效果:可能增加休息代謝率與能量消耗;減重的作用沒有一致的結果
研究證據
有幾個人體研究已經研究苦橙對減重的效果( Ref. 23 )。不過這些研究裡面,苦橙大多是和其他減重成分一起組成配方,所以很難以釐清到底是哪個發揮了作用。
有一個以 20 位健康但過重的成年人為對象的研究,隨機分成減重組、安慰劑組或什麼都沒做組,為期 6 週,減重組補充的配方是每天 975 毫克的苦橙萃取物、 528 毫克的咖啡因以及 900 毫克的聖約翰草,安慰劑組也會服用膠囊,但裡面不有任何功效成分,而什麼都沒做組就真的什麼都沒做了。
所有參與者在研究期間都會接受體能訓練課程,並規定每天攝取 1,800 大卡。試驗結束後,減重組比安慰劑與什麼都沒做組減少較多體脂,增加較多基礎代謝率。這三組參與者的體重都有減下來,但作者並沒有提到減重組(減少 1.4 公斤)和安慰劑組( 0.9 公斤)及什麼都沒做組( 0.4 公斤)之間是否有顯著差異( Ref. 24 )。
另外有個研究找來 8 位過重或肥胖的健康成年人參與,經過諮詢後讓他們採行每天 1,200 – 1,500 大卡的飲食計畫,並且隨機安排他們服用含苦橙減重配方補充品或安慰劑,減重配方每天會攝取到的成份有苦橙萃取物(含 18 毫克的 synephrine )、瓜拿納萃取物(含咖啡因 396 毫克)。結果發現,研究過程中減重組的休息代謝率顯著比安慰劑組高,不過在 8 週的研究結束之後,兩組的休息代謝率則是沒有顯著差異。在研究最後一天,減重組的體重平均增加了 1.13 公斤,而安慰劑組增加 0.09 公斤,不過增加的體重並沒有影響到體脂與瘦肉組織或腰圍。
2012 年有一篇回顧 23 個小規模人類臨床試驗的研究,總共涵蓋了 360 位受試者,總結到苦橙萃取物能增加休息代謝率與能量消耗( Ref. 24 )。
安全性
含有苦橙的產品可能會有安全性的疑慮。有研究告報指出苦橙的副作用有胸痛、頭痛、焦慮、心跳加速、骨骼肌不適、心室顫動、缺血性中風、心肌梗塞還有死亡( Ref. 25, 26 )。
不過許多產品是多種本草的複方配方,因此沒辦法確定這些副作用就一定是苦橙造成。有些研究指出苦橙與 synephrine (苦橙萃取物)會使血壓升高與心率增加,但也有些研究沒有這些副作用( Ref. 19, 20, 21, 22, 27, 28, 29, 30, 31 )。舉例來說,讓 15 位健康的男女攝取苦橙萃取物與安慰劑,苦橙的劑量是 900 毫克的苦橙萃取物(含 54 毫克 synephrine ),結果發現服用後 5 小時間,苦橙組的收縮壓、舒張壓顯著高於安慰劑組( Ref. 30 )。
然而,在一個有 80 位健康男性參與的 8 週臨床試驗,他們有做阻力訓練的習慣,試驗期間每天補充含有苦橙抽出物的補充品,成分有 20 毫克 synephrine 、 284 毫克的咖啡因,以及其他成分,結果受試者們並沒有出現心率、收縮壓或舒張壓增加的副作用( Ref. 32 )。
有些研究者認為苦橙萃取物很可能不是直接的心血管刺激劑( Ref. 21, 30, 31 ),反之,很可能是配方裡的咖啡因、其他可能刺激成分,或是苦橙萃取物裡的其他分子導致。 ▴ Back
咖啡因
許多幫助減重的膳食補充品會添加咖啡因或是含咖啡因的植物,例如瓜拿納。綠茶和其它茶也含有咖啡因。有些減重補充品標示上不會標示咖啡因含量,只列出和含有它的植物名稱。因此,消費者可能在不知不覺中就吃到含有咖啡因的減重食品( Ref. 33 )。
咖啡因能刺激中樞神經系統、心臟、骨骼肌。它也會增加胃酸與結腸的活動,另外也有利尿的作用。咖啡因的半衰期大概是 6 個小時,在攝取之後的 15-45 分鐘內血中的濃度會增加,約在 60 分鐘左右達到最高峰( Ref. 34 )。
人類攝取咖啡因會增加生熱效應,且隨攝取量而有線性增加的關係。比較健康成年人攝取 100 毫克的咖啡因與安慰劑之後的能量消耗,咖啡因組平均的能量消耗會比安慰劑組增加 9.2 大卡/小時,而這個效果能持續 3 小時以上。咖啡因幫助減重的作用是藉由刺激中樞神經的交感神經活化來增加脂肪氧化,以及增加體液的排出( Ref. 33 )。不過習慣接觸咖啡因可能會造成咖啡因耐受性增加,因而抵消它的減重效果。
減重效果:對體重或減少長期體重可能有些微的作用
研究證據
咖啡因會增加能量消耗與脂質氧化作用( Ref. 34 ),只是這個作用在減重上能發揮多少作用,目前還不是很清楚就是了,原因在於部分關於咖啡因對減重的臨床試驗的時間都很短,而且不是單純使用咖啡因進行。
有個研究有 167 位過重與肥胖的參與者,每天吃含有 192 毫克咖啡因的可樂豆與麻黃(含 90 毫克的麻黃素)或安慰劑。研究者會建議參與者吃限制每日脂肪的卡路里不超過 30% 的飲食,並且適度的運動。六個月後,咖啡因組體重平均減少 5.3 公斤,而安慰劑組平均減少 2.6 公斤,而且與安慰劑相比,咖啡因組的體脂肪顯著減少( Ref. 35 )。
日本有個臨床試驗,所使用的咖啡因補充品,除了含有咖啡因,另外添加了萃取自柑桔類果皮的葡糖基橙皮苷( Glucosyl Hesperidin )。有 75 位健康但體重過重的男女參與者了 12 週的試驗,期間飲食與生活型態維持原本的樣子,並隨機把他們分配到安慰劑與四種試驗因配方,分別是咖啡因 0 、 25 、 50 與 75 毫克加上 500 毫克的葡糖基橙皮苷。結果發現 75 毫克咖啡因組 BMI 的減少明顯比安慰劑多,分別減 0.56 與 0.02 公斤/身高2。與安慰劑組相比,50 毫克與 75 毫克兩組的腹部脂肪明顯減少,不過另外兩組不管是在 BMI 還是腹部脂肪就都沒有顯著差異。從這個研究的發現來看,主要發揮作用的很可能是咖啡因( Ref. 36 )。
有個為期 12 年的前瞻觀察研究,讓我們能用更長的時間來看咖啡因攝取與體重之間的關係( Ref. 37 )。研究者追蹤 18,417 位健康的男性,以及 39,470 位健康的女性。平均來看,參與者在研究期間體重增加了一些,不過這 12 年間咖啡因攝取增加的男性平均體重會比咖啡攝取減少的男性要少 0.43 公斤。那女性呢?咖啡因攝取增加的女性平均體重會比咖啡因攝取減少要少 0.35 公斤。
安全性
成人每天攝取不到 400-500 毫克通常不太會有安全性的問題。參與者回報的副作用有神經質、神經過敏、嘔吐,以及心跳太快。 ▴ Back
肉鹼( Carnitine )

肉鹼是好幾種化合物的集合名詞,包含 L-肉鹼、醯基肉鹼,以及丙醯-L-肉鹼。它是由離胺酸( lysine )和甲硫胺酸( methionine )構成。肉鹼天然存在於肉、魚、禽肉,還有乳製品裡,但少量存在於植物食物。人類能自己從組成的胺基酸合成肉鹼,因此一般認為不需要額外補充肉鹼。
幾乎所有身體的細胞裡都有肉鹼,能幫助脂肪酸運輸進入粒線體,幫助脂肪酸進行 beta-氧化作用。也因為這些作用的關係,肉鹼被認為可以用在減重用途上。
減重效果:可能有些微減重的效果
研究證據
現在已經有主要評估肉鹼對血脂、心血管疾病與第二型糖尿病效果的研究,但對於減重,大部分的研究是放在次要的結果。一篇以 258 位未控制的第二型糖尿病患者為對象的臨床試驗,每天給予 2 公克的 L-肉鹼和羅氏鮮( 360 毫克),研究進行時間是 1 年,結果發現肉鹼與羅氏鮮一起使用的減重效果會比僅使用羅氏鮮好( Ref. 38 )。
不過,有個每天僅食用 2 公克的 L-肉鹼,為期 6 個月的研究,總共有 94 位過重新診斷罹患第二型糖尿病的男女,結果發現肉鹼不影響體重的變化( Ref. 39 )。
2016 年有篇系統回顧與薈萃分析統合了 9 篇以成人為對象的肉鹼補充品的臨床試驗。總共含括 911 位參與者,當中 8 篇試驗, L-肉鹼的劑量範圍從 1.8 到 4 公克,研究的長度從 30 到 360 天;另外有一篇, L-肉鹼的劑量設計是每天每公斤體重 15 毫克,研究時間是 182 天。整體來看,相對於安慰劑組,補充肉鹼的人體重平均減少超過 1.33 公斤。但實際上肉鹼對減重的效果如何就得要更多的研究才能確定( Ref. 40 )。
安全性
研究發現每天吃 4 公克的肉鹼的耐受性是好的,不過肉鹼可能導致噁心、嘔吐、腹部絞痛、腹瀉,還有身體會有魚臭味( Ref. 41, 42 )。很少的情況下,患有尿毒症與癲癇發作的人會有肌肉虛弱的副作用。
有些研究指出小腸的細菌會把肉鹼代謝成氧化三甲胺( trimethylamine N-oxide , TMAO ),這個分子可能會增加心血管疾病的風險( Ref. 43 )。這種情形吃葷的人會比吃素的常見。至於為什麼會有這種情形呢?現在還不是很明白當中的機制。 ▴ Back
鉻( Chromium )
這裡所指的鉻是三價鉻,是人體需要的微量礦物質,而它可能有助於胰島素發揮作用。研究發現體內鉻的狀態不佳可能影響葡萄糖的耐受性以及第二型糖尿病( Ref. 44 )。
有些研究指出補充鉻可能也有助於減少食物的攝取、飢餓程度與對脂質的渴望,不過這些作用的研究資料還不多( Ref. 45 )。
減重效果:對體重與體脂肪的效果很小
研究證據
有幾個研究已評估有關補充鉻在減重上的效果。 2013 年有篇回顧分析了 9 個使用吡啶甲酸鉻( chromium picolinate )的隨機控制試驗,總共有 622 位過重或肥胖的人參與( Ref. 46 )。
試驗時間從 8 週到 6 個月,吡啶甲酸鉻的劑量從每天 200 到 1,000 微克。有 6 個試驗有加入阻力訓練或重量訓練,而另外三個則沒有加入鍛鍊的項目。與安慰劑相比,吡啶甲酸鉻組的體重減少了 1.1 公斤,但體重減少量與吡啶甲酸鉻的劑量多寡沒有顯著的關係。研究者認為鉻補充在減重上的臨床結果有待商確,而且整體證據的品質低。
2013 年還有一篇系統回顧與薈萃分析研究( Ref. 47 ),回顧 11 篇隨機控制試驗,當中也包含了大部分上述回顧的研究。此研究評估 866 位過重會肥胖的人補充鉻對減重的效果。結果發現 8 到 26 週,每天 137 到 1,000 微克的鉻補充能減少 0.5 公斤的體重和 0.46% 的體脂,這篇研究作者的結論和上一段的回顧研究結果類似,鉻補充對減重的作用很小且臨床意義不確定。
安全性
在建議攝取量下沒有安全上的疑慮,這裡所指的建議攝取量是美國的適當攝取量,給沒有懷孕與哺乳的成人建議是每天 20-35 微克。參與者回報的副作用有頭痛、水樣便、便秘、虛弱、眩暈、噁心、嘔吐,以及蕁麻疹。
目前台灣的國人膳食營養素參考攝取量裡並沒有鉻的建議或參考,不過在食品添加物裡,含有鉻的營養添加劑可添加於膠囊或錠狀的食品,每日攝取量不得高於 200 微克。 ▴ Back
共軛亞油酸( Conjugated Linoleic Acid )
共軛亞油酸(簡稱 CLA )是一種含有共軛雙鍵的亞油酸( linoleic acid )異構物的混合物,常見於乳製品與牛肉。 CLA 的異構物包含 c9t11-CLA 和 t10c12-CLA , CLA 前面接的 c9t11 表示第 9 個碳的雙鍵是順式,第 11 個碳的雙鍵是反式。除了乳製品或牛肉含有 CLA ,減重補充品裡的 CLA 通常來萃取自紅花籽油( Ref. 48 )。
研究者發現 CLA 能增加骨骼肌的脂肪分解與脂肪酸氧化,因此認為它有減重的潛力( Ref. 49, 50 )。
減重效果:對體重與體脂的作用很小
科學證據
雖然從 CLA 在動物實驗似乎有減少體脂的作用( Ref. 49 ), 但人類研究的成效確很小,而臨床意義還不明確( Ref. 51 )。有個雙盲、安慰劑控制試驗評估 180 位過重的男女補充 CLA 1 年的效果。研究不限制參與者的飲食,可自己喜好選擇,試驗分成三組,分別是每天 3.6 公克的游離型 CLA 、 3.4 公克的三酸甘油酯型 CLA ,以及安慰劑組。研究結束的時候,與安慰劑組相比,兩組 CLA 的體脂均顯著下降,平均分別減少了 6.9% 和 8.7% 。此外,補充游離型 CLA 組的瘦肉組織也顯著比安慰劑組高。
另外有個以 35 位肥胖停經且患有第二型糖尿病女性為對象的雙盲交叉試驗,連續 16 週每天補充 CLA 6.4 公克,結果發現,與補充葵花油相比,補充 CLA 顯著減少受試者的 BMI 與總體脂肪( Ref. 52 )。
這兩篇研究的結果和 2012 年的一篇隨機、雙盲、安慰劑控制的小型試驗類似,總共有 63 位過重或肥胖成年人參與,試驗進行了 12 週,分成每天 3.4 公克的 CLA 和安慰劑組,結果發現與研究一開始相比,CLA 組的體重與體脂顯著減少,分別減了 0.69 公斤和 0.49 公斤;而安慰劑組試驗前後的體重與體脂並沒有出現顯著的差異( Ref. 53 )。
此外,有研究讓 28 位年輕肥胖女性,連續 8 週,每天補充 3.2 公克的 CLA 或安慰劑並結合有氧運動,結果發現 CLA 組並沒有比安慰劑組減去更多的體脂( Ref. 54 )。
在一篇回顧 7 篇隨機控制試驗的系統回顧與薈萃分析裡, CLA 補充的劑量從每天 2.4 到 6 公克,研究時間從 6 到 12 個月,與安慰劑相比,補充 CLA 能減少 0.7 公斤的體重和 1.33 公斤的體脂。不過,該研究的作者強調這些研究的臨床意義還不夠確定( Ref. 51 )。
安全性
CLA 似乎耐受性良好。大部分報告裡出現的副作用輕微,腹部不適與疼痛、便秘、腹瀉、噁心、嘔吐,以及消化不良。此外,CLA 可能會讓一些氧化壓力指標上升,並且減少母乳脂肪量,不過這些作用得要有更多的研究才能確認( Ref. 55 )。
補充說明
在台灣,含有 CLA 或紅花籽油的食品還滿常見的,只是呢!實驗給參與者補充的劑量都是幾公克的等級,但如果你去市面上隨便挑一款主打 CLA 的產品來看,可能得要特別注意每日的食用量,確定一天能攝取到多少 CLA 會比較好。 ▴ Back
藤黃果( Garcinia cambogia / hydroxycitric acid )

藤黃果是一種生長在亞洲、非洲與波利尼西亞群島的果樹。果肉與果皮富含羥基檸檬酸( Hydroxycitric acid ,簡稱 HCA ),而這也是一般認為藤黃果在減重上的主要功效成分,能抑制脂質生成、增加肝臟的肝糖合成,並且抑制食慾與減少體重( Ref. 56, 57 )。
減重效果:減重的作用很小
研究證據
從老鼠的研究發現藤黃果有抑制食物攝取與體重增加的作用( Ref. 58, 59 )。不過從人類身上取得的減重證據就不那麼確定,有效無效的結果都有,而且就算有效,實際的作用也有限。
在一篇隨機、安慰劑控制試驗中,有 89 位過重的女性,隨機分配她們每天補充 2.4 公克的 HCA 或安慰劑,並吃一日 1,200 大卡的飲食,連續 12 週。結果發現補充 HCA 女性的體重明顯比安慰劑組減得多,分別減少了 3.7 公斤與 2.4 公斤。不過在這個試驗裡並沒有觀察到藤黃果有對食慾產生影響( Ref. 60 )。
另外有篇以 135 位過重男女為對象的雙盲、安慰劑控制試驗,讓受試者每天三餐餐前補充安慰劑或 1,000 毫克的藤黃果抽出物,一日總共攝取量是 3,000 毫克的藤黃果抽出物,內含 1,500 毫克的 HCA ,飲食採高纖低卡路理的設計,試驗進行時間是 12 週。研究結束後,兩組受試者的體重都減少了,不過兩組之間的體重減少並沒有出現顯著的差異( Ref. 61 )。
2011 年有篇回顧與薈萃分析研究分析了 12 篇隨機控制試驗,總共有 706 位參與者參與。其中有 9 個試驗指出每天補充 1,000 到 2,800 毫克的 HCA 2 到 12 週,與安慰劑相比,補充 HCA 者的體重減少 0.88 公斤。不過作者強調在這篇回顧研究中大部分試驗都有研究方法的問題,從方法較嚴謹的兩篇試驗來看的話,HCA 的劑量分別是每天 1,500 毫克和 2,800 毫克,補充 HCA 對減重就沒有達到顯著效果( Ref. 59 )。2013 年有篇回顧研究的作者也有類似的結論,因此要確認藤黃果/HCA 是否真的有助減重的話,仍需要更大規模與長期的臨床試驗證實才行( Ref. 62 )。
安全性
關於藤黃果或 HCA 副作用的研究報告通常是輕微的,包含頭痛、噁心、上呼吸道不適,以及腸胃不適。此外,曾有試驗出現 3 例因補充藤黃果而出現焦躁的案例,會有這樣的情形很可能和 HCA 的血清素活性( serotonergic activity )有關( Ref. 63 )。 ▴ Back
綠咖啡豆萃取物( Green Coffee Bean Extract )

咖啡植物( Coffea arabica, Coffea canephora, Coffea robusta )的種子在烤焙之前是綠色的,因而稱作綠咖啡豆。不同與烤焙過的咖啡豆,綠咖啡豆的綠原酸( chlorogenic acid )含量較多。老鼠與人類的試驗中發現綠原酸可能藉調節脂肪合成來抑制體內脂肪的堆積( Ref. 64, 65 )。另外,綠咖啡豆萃取物可能減少小腸對葡萄糖的吸收,而有調節葡萄糖代謝的作用( Ref. 66 )。
減重效果:對體重可能有一些作用
科學證據
綠咖啡豆結合高脂飲食的老鼠試驗發現能顯著減少老鼠的體重增加與體脂肪( Ref. 64, 65 )。目前以人為對象的綠咖啡豆臨床試驗的數量僅有一些,而且所有試驗的研究方法品質都不夠好。有一篇包含了三個試驗的薈萃分析,體重過重的人每天攝取 180 或 200 毫克的綠咖啡豆萃取物,研究時間 4 到 12 週。結論是綠咖啡豆萃取物對體重的作用有一些作用,與安慰劑相比,吃綠咖啡豆能讓體重平均多減少 2.47 公斤,不過作者有提到這些研究的品質不夠好,因此無法確定綠咖啡豆萃取物在減重上的效果( Ref. 66 )。
安全性
人們對綠咖啡抽出物的耐受性似乎是好的,不過它的安全性還沒經過嚴格研究。相關研究中出現過的副作用有頭痛和泌尿道感染( Ref. 66 )。如果綠咖啡豆抽出物是沒有去除咖啡因的類型,那麼也可能會有咖啡因相關的副作用。 ▴ Back
綠茶與綠茶抽出物( Green Tea and Green Tea Extract )

綠茶是我們生活周遭很容易就可取得的飲料,也有很多它關於健康好處的研究。除了當茶喝,綠茶也會以萃取物的形式,做成膳食補充品的型態。綠茶裡有關減重的活性成分是咖啡因與兒茶素,主要是表沒食子兒茶素沒食子酸酯( Epigallocatechin gallate , EGCG ),是一種黃酮類化合物( Ref. 67 )。
通常一杯綠茶約含有 240 到 320 毫克的兒茶素與和 45 毫克的咖啡因( Ref. 67 )。一般認為綠茶還有它的能份可能有助於增加能量消耗與脂質的氧化作用,以及減少脂質生成和脂質吸收等作用,因而可應用在減重的用途上( Ref. 68, 69, 70, 71 )。此外,綠茶也可能有減少碳水化合物的消化與吸收的作用( Ref. 72 )。
減重效果:可能對體重有些作用
科學證據
關於綠茶兒茶素在減重與維持體重的作用,已經有好幾篇人類的研究發表。 2012 年有一篇回顧研究分析了 14 篇綠茶萃取物的隨機控制試驗,試驗時間 12 到 13 週,總共有 1,562 位過重或肥胖的人參與,綠茶兒茶素的劑量範圍從 141 到 1,207 毫克。 14 篇研究裡面有 10 篇的綠茶抽出物產品有含咖啡因。結果發現綠茶能比安慰劑平均多減 0.95 公斤,但如果把研究品質較差的試驗去掉,再進行分析的話,綠茶與安慰劑之間的體重就沒有顯著差異了( Ref. 73 )。
另外一篇分析了 15 篇隨機試驗的系統回顧與薈萃分析,當中有 6 篇試驗了有或無添加咖啡因和綠茶兒茶素,咖啡因的劑量是每天 39 到 83 毫克,兒茶素的劑量是 576 到 690 毫克。結果發現有咖啡因的減重效果較好,體重比無咖啡因平均多減了 1.38 公斤。 15 篇研究裡,只有兩篇是單獨評估綠茶兒茶素的功效,結果是綠茶兒茶素的補充不影響參與者的體重( Ref. 74 )。
後來也有用去咖啡因的綠茶抽出物做的研究,每天攝取的總兒茶素量是 1,315 毫克,試驗以 121 位過重或肥胖的停經女性為對象,進行了 12 個月,結果發現綠茶萃取物對體重、 BMI 或腰圍並沒有顯著的作用( Ref. 75 )。
有一篇包含了 11 篇隨機控制試驗的薈萃分析研究,發現補充 EGCG 與咖啡因, 12 到 13 週,綠茶組顯著比安慰劑組多減 1.31 公斤的體重( Ref. 76 )。
歐洲食品安全局( EFSA )在 2010 年檢查有關於綠茶的健康宣稱,結論是補充綠茶兒茶素(含 EGCG )和維持或達成正常體重之間並沒有因果關係( Ref. 77 )。總結來說,如果綠茶真的有助於減重的話,那麼它的作用應該很小,而且很可能沒有臨床顯著的意義。
安全性
一般當茶喝沒有副作用( Ref. 67 )。但綠茶抽出物就可能會有,大多數報告發生的副作用有噁心、便秘、腹部不適和血壓( Ref. 78 )。
老鼠毒性試驗的結果顯示綠茶抽出物並不會引起癌症,但確實會引起許多部位的非腫瘤性病變,包含鼻子、肝,以及骨髓( Ref. 79 )。
其他老鼠的證據顯示高劑量的兒茶素可能引起肝損傷。在人類補充綠茶抽出物的研究上,有越多越多的證據指出可能引起肝損傷,但為什麼會這樣的原因依然不明。一篇以 1,021 位停經女性為對象的研究,讓參與者每天攝取 1,315 毫克的兒茶素(含 843 毫克 EGCG )和 15.8 毫克的咖啡因,研究進行了 12 個月,結果發現綠茶組的肝酵素明顯比安慰劑組多,而且有些女性發展成稍微或嚴重的肝功能異常( Ref. 80 )。
另外有研究讓健康的男性連續三週每天補充 714 毫克的綠茶多酚,發現這樣的攝取量並不會增加肝酵素的量或引起肝功能異常( Ref. 81 )。
從 2006 年至今,補充綠茶抽出物與肝損傷的案例至少有 50 件報告( Ref. 82 )。 2008 年美國藥典( USP )系統回顧了綠茶產品的安全性,以 34 個肝損傷案例與動物藥理和毒理資訊為基礎, USP 的結論是綠茶產品很可能導致 7 個肝損傷,以及可能引起 27 例肝損傷。 USP 提到問題很可能是空腹服用綠茶萃取物,因此建議和其他食物一起補充綠茶抽出物能把導致肝損傷的風險降到最低( Ref. 83 )。 ▴ Back
益生菌( Probiotics )
人體內外有著許多我們看不到的微生物,而這些微小生命的數目更是人本身細胞的 10 倍以上,它們不僅只是住在人類的身上,可能從許多方面影響了我們的健康( Ref. 84, 85 )。
雖然微生物遍佈人類的身體,但絕大部分住在結腸裡面,一般以腸道微生物稱呼,它們能幫助宿主從食物萃取營養素與能量。老鼠試驗的結果支持腸道微生物不僅影響飲食的能量利用,也會影響宿主對能量的利用與貯存( Ref. 86 )。
不過這個作用對人是否也是如此就還不是很確定。不過,調整腸道微生物已經被用作預防或治療人類肥胖,最常見的方式就是補充益生菌了。優格、其他乳製品以及部分發酵食物是我們日常生活中常見的益生菌食物來源。益生菌的品種有很多,包含乳桿菌屬( lactobacilli )、鏈球菌屬( streptococci )和雙歧桿菌屬( bifidobacteria ),在體內有廣泛的作用( Ref. 85, 86 )。
減重效果:對體脂、腰圍與臀圍,或體重的影響很小
科學證據
大部分有關益生菌對腸道微生物影響以及減重試驗的對象大多是老鼠,從這些試驗的結果看來,益生菌在減重上似乎是可行的方法。有個研究讓肥胖老鼠吃高脂飲食,益生菌的補充顯著減少牠們體重,還有脂肪的堆積( Ref. 87 )。
至於人類的臨床研究的數目就相當有限,而且結果並不一致。一項為期 12 週有 210 位成年人參與的隨機試驗,研究者讓他們隨機補充每公克含有 107 、 106 或 0 CFU Lactobacillus gasseri SBT2055 ( LG2055 )的發酵牛乳。 CFU 是 colony-forming units 的縮寫,中文的意思是菌落形成單位,是用來計算細菌數量的方法,數字越高細菌數越多。結果發現 107 、 106 LG2055 組的腹部脂肪、 BMI 、腰圍和臀圍,和體脂肪等,下降得比控制組多( Ref. 88 )。
不過,有一篇包含 4 個隨機控制試驗的系統回顧與薈萃分析的研究,結果發現補充益生菌對體重或 BMI 沒有顯著的差異。研究者強調研究的數量和樣本數都太少,而且研究方法的品質也不夠好,因此無法給出個肯定的結論。未來還需要更大規模的研究來確定益生菌對人類肥胖是否有改善作用( Ref. 89 )。
安全性
對身體健康的人來說,不管是來自食物還是補充品的益生菌都很安全( Ref. 88, 89 )。而在臨床試驗裡,曾有副作用的報告,但不嚴重,例如輕微的脹氣( Ref. 90 )。 ▴ Back
 這次的分享就先到此為止,雖然還有許多減重成分沒有被討論到,未來有機會再另外寫文章探討。如果你從頭看到尾,我們要先深深的給您鞠躬,感謝你讀完,另外,你看完之後腦中殘留的概念八成是「小」、「一些」之類的結論吧!或許你也會想,為什麼效果都這麼「微小」又「微妙」呢?
這次的分享就先到此為止,雖然還有許多減重成分沒有被討論到,未來有機會再另外寫文章探討。如果你從頭看到尾,我們要先深深的給您鞠躬,感謝你讀完,另外,你看完之後腦中殘留的概念八成是「小」、「一些」之類的結論吧!或許你也會想,為什麼效果都這麼「微小」又「微妙」呢?
首先,不管是什麼好棒棒的減重成分,本質上都是食品。在上一篇我們有提過體重是多重因素相互影響之後的結果,不是簡單的改變一個生活變項就能帶來巨大的成效,人生在世,不管是要得到什麼都是要付出代價的呀。
在文章最後要強調一件事情!我們並不是故意要把所有減重產品打成無效,而是在回顧這麼多文獻之後,結論就是如此。很多產品會強調從某一個單一試驗鐘,發現了很好的減重數字,但事實上,一個減重成分或是其他保健成分到底有沒有效,是要經過重重檢驗!結果能被重新驗證、實驗設計品質良好、參與的人數/種族多…當有足夠的證據支持的時候,科學家才會稍微肯定的說某某成分可能有用。
舉個例子,只有單一廠商或單一科學家,做出一系列的研究都說有效,但其他人重複了實驗結果都沒效,那我們要相信哪一個呢?正常的狀況下,我們可能會傾向後者,因為前者的利益衝突通常太大了啊!
這篇文章回顧了整整 90 篇文獻,回顧到眼睛都要脫窗了。希望大家可以分享給身邊的朋友,至少讓大家在挑選產品時,能夠有些具有真正科學意義的參考喔!
Reference
- National Institutes of Health – office of Dietary Supplements – Dietary Supplements for Weight Loss
- Davies, K. M., Heaney, R. P., Recker, R. R., Lappe, J. M., Barger-Lux, M. J., Rafferty, K., & Hinders, S. (2000). Calcium intake and body weight. The Journal of Clinical Endocrinology & Metabolism, 85(12), 4635-4638.
- Heaney, R. P. (2003). Normalizing calcium intake: projected population effects for body weight. The Journal of nutrition, 133(1), 268S-270S.
- Parikh, S. J., & Yanovski, J. A. (2003). Calcium intake and adiposity. The American journal of clinical nutrition, 77(2), 281-287.
- Zemel, M. B., Shi, H., Greer, B., Dirienzo, D., & Zemel, P. C. (2000). Regulation of adiposity by dietary calcium. The FASEB Journal, 14(9), 1132-1138.
- Villarroel, P., Villalobos, E., Reyes, M., & Cifuentes, M. (2014). Calcium, obesity, and the role of the calcium-sensing receptor. Nutrition reviews, 72(10), 627-637.
- Christensen, R., Lorenzen, J. K., Svith, C. R., Bartels, E. M., Melanson, E. L., Saris, W. H., … & Astrup, A. (2009). Effect of calcium from dairy and dietary supplements on faecal fat excretion: a meta‐analysis of randomized controlled trials. Obesity reviews, 10(4), 475-486.
- Jacobsen, R., Lorenzen, J. K., Toubro, S., Krog-Mikkelsen, I., & Astrup, A. (2005). Effect of short-term high dietary calcium intake on 24-h energy expenditure, fat oxidation, and fecal fat excretion. International journal of obesity, 29(3), 292.
- Vartanian, L. R., Schwartz, M. B., & Brownell, K. D. (2007). Effects of soft drink consumption on nutrition and health: a systematic review and meta-analysis. American journal of public health, 97(4), 667-675.
- Jeukendrup, A. E., & Randell, R. (2011). Fat burners: nutrition supplements that increase fat metabolism. Obesity reviews, 12(10), 841-851.
- Peng, J., Yuan, J. P., Wu, C. F., & Wang, J. H. (2011). Fucoxanthin, a marine carotenoid present in brown seaweeds and diatoms: metabolism and bioactivities relevant to human health. Marine drugs, 9(10), 1806-1828.
- van Heerden, F. R., Horak, R. M., Maharaj, V. J., Vleggaar, R., Senabe, J. V., & Gunning, P. J. (2007). An appetite suppressant from Hoodia species. Phytochemistry, 68(20), 2545-2553.
- Bredsdorff, L., Wedebye, E. B., Nikolov, N. G., Hallas-Møller, T., & Pilegaard, K. (2015). Raspberry ketone in food supplements–High intake, few toxicity data–A cause for safety concern?. Regulatory Toxicology and Pharmacology, 73(1), 196-200.
- Ríos-Hoyo, A., & Gutiérrez-Salmeán, G. (2016). New dietary supplements for obesity: what we currently know. Current obesity reports, 5(2), 262-270.
- Earthman, C. P., Beckman, L. M., Masodkar, K., & Sibley, S. D. (2012). The link between obesity and low circulating 25-hydroxyvitamin D concentrations: considerations and implications. International journal of obesity, 36(3), 387.
- Ngondi JL, Etoundi BC, Nyangono CB, Mbofung CM, Oben JE. IGOB131, a novel seed extract of the West African plant Irvingia gabonensis, significantly reduces body weight and improves metabolic parameters in overweight humans in a randomized double-blind placebo controlled investigation. Lipids Health Dis 2009;8:7.
- Onakpoya I, Davies L, Posadzki P, Ernst E. The efficacy of Irvingia gabonensis supplementation in the management of overweight and obesity: a systematic review of randomized controlled trials. J Diet Suppl 2013;10:29-38.
- Ozkan G, Ulusoy S. A case of renal failure developing in association with African mango consumption. Int J Clin Exp Med 2015;8:6374-8.
- Haaz, S., Fontaine, K. R., Cutter, G., Limdi, N., Perumean‐Chaney, S., & Allison, D. B. (2006). Citrus aurantium and synephrine alkaloids in the treatment of overweight and obesity: an update. Obesity reviews, 7(1), 79-88.
- Seifert, J. G., Nelson, A., Devonish, J., Burke, E. R., & Stohs, S. J. (2011). Effect of acute administration of an herbal preparation on blood pressure and heart rate in humans. International journal of medical sciences, 8(3), 192.
- Stohs, S. J., Preuss, H. G., & Shara, M. (2011). The safety of Citrus aurantium (bitter orange) and its primary protoalkaloid p‐synephrine. Phytotherapy Research, 25(10), 1421-1428.
- Roman, M. C., Betz, J. M., & Hildreth, J. (2007). Determination of synephrine in bitter orange raw materials, extracts, and dietary supplements by liquid chromatography with ultraviolet detection: single-laboratory validation. Journal of AOAC International, 90(1), 68-81.
- Stohs, S. J., Preuss, H. G., & Shara, M. (2012). A review of the human clinical studies involving Citrus aurantium (bitter orange) extract and its primary protoalkaloid p-synephrine. International journal of medical sciences, 9(7), 527.
- Bent, S., Padula, A., & Neuhaus, J. (2004). Safety and efficacy of Citrus aurantium for weight loss. The American journal of cardiology, 94(10), 1359-1361.
- Onakpoya, I., Davies, L., & Ernst, E. (2011). Efficacy of herbal supplements containing Citrus aurantium and synephrine alkaloids for the management of overweight and obesity: a systematic review. Focus on Alternative and Complementary Therapies, 16(4), 254-260.
- Stohs, S. J. (2010). Assessment of the adverse event reports associated with Citrus aurantium (bitter orange) from April 2004 to October 2009. Journal of Functional Foods, 2(4), 235-238.
- Colker, C. M., Kalman, D. S., Torina, G. C., Perlis, T., & Street, C. (1999). Effects of Citrus aurantium extract, caffeine, and St. John’s wort on body fat loss, lipid levels, and mood states in overweight healthy adults. Current Therapeutic Research, 60(3), 145-153.
- Kaats, G. R., Miller, H., Preuss, H. G., & Stohs, S. J. (2013). A 60 day double-blind, placebo-controlled safety study involving Citrus aurantium (bitter orange) extract. Food and Chemical Toxicology, 55, 358-362.
- Haller, C. A., Benowitz, N. L., & Jacob III, P. (2005). Hemodynamic effects of ephedra-free weight-loss supplements in humans. The American journal of medicine, 118(9), 998-1003.
- Bui, L. T., Nguyen, D. T., & Ambrose, P. J. (2006). Blood pressure and heart rate effects following a single dose of bitter orange. Annals of Pharmacotherapy, 40(1), 53-57.
- Hansen, D. K., George, N. I., White, G. E., Pellicore, L. S., Abdel-Rahman, A., Fabricant, D., & Food and Drug Administration. (2012). Physiological effects following administration of Citrus aurantium for 28 days in rats. Toxicology and applied pharmacology, 261(3), 236-247.
- Jung, Y. P., Earnest, C. P., Koozehchian, M., Cho, M., Barringer, N., Walker, D., … & Kreider, R. B. (2017). Effects of ingesting a pre-workout dietary supplement with and without synephrine for 8 weeks on training adaptations in resistance-trained males. Journal of the International Society of Sports Nutrition, 14(1), 1.
- Manore, M. M. (2012). Dietary supplements for improving body composition and reducing body weight: where is the evidence?. International journal of sport nutrition and exercise metabolism, 22(2), 139-154.
- Harpaz, E., Tamir, S., Weinstein, A., & Weinstein, Y. (2017). The effect of caffeine on energy balance. Journal of basic and clinical physiology and pharmacology, 28(1), 1-10.
- Boozer, C. N., Daly, P. A., Homel, P., Solomon, J. L., Blanchard, D., Nasser, J. A., … & Meredith, T. (2002). Herbal ephedra/caffeine for weight loss: a 6-month randomized safety and efficacy trial. International Journal of Obesity, 26(5), 593.
- Ohara, T., Muroyama, K., Yamamoto, Y., & Murosaki, S. (2016). Oral intake of a combination of glucosyl hesperidin and caffeine elicits an anti-obesity effect in healthy, moderately obese subjects: a randomized double-blind placebo-controlled trial. Nutrition journal, 15(1), 6.
- Lopez-Garcia, E., van Dam, R. M., Rajpathak, S., Willett, W. C., Manson, J. E., & Hu, F. B. (2006). Changes in caffeine intake and long-term weight change in men and women–. The American journal of clinical nutrition, 83(3), 674-680.
- Derosa, G., Maffioli, P., Ferrari, I., D’Angelo, A., Fogari, E., Palumbo, I., … & Cicero, A. F. (2010). Orlistat and L-carnitine compared to orlistat alone on insulin resistance in obese diabetic patients. Endocrine journal, 57(9), 777-786.
- Derosa, G., Cicero, A. F., Gaddi, A., Mugellini, A., Ciccarelli, L., & Fogari, R. (2003). The effect of L-carnitine on plasma lipoprotein (a) levels in hypercholesterolemic patients with type 2 diabetes mellitus. Clinical therapeutics, 25(5), 1429-1439.
- Pooyandjoo, M., Nouhi, M., Shab‐Bidar, S., Djafarian, K., & Olyaeemanesh, A. (2016). The effect of (L‐) carnitine on weight loss in adults: a systematic review and meta‐analysis of randomized controlled trials. Obesity reviews, 17(10), 970-976.
- Villani, R. G., Gannon, J., Self, M., & Rich, P. A. (2000). L-Carnitine supplementation combined with aerobic training does not promote weight loss in moderately obese women. International journal of sport nutrition and exercise metabolism, 10(2), 199-207.
- Shils, M. E., & Shike, M. (Eds.). (2006). Modern nutrition in health and disease. Lippincott Williams & Wilkins.
- Koeth, R. A., Levison, B. S., Culley, M. K., Buffa, J. A., Wang, Z., Gregory, J. C., … & Tang, W. W. (2014). γ-Butyrobetaine is a proatherogenic intermediate in gut microbial metabolism of L-carnitine to TMAO. Cell metabolism, 20(5), 799-812.
- Copper, I. O. M. (2001). Dietary reference intakes for vitamin A vitamin K, arsenic, boron, chromium, copper, iodine, iron, manganese, molybdenum, nickel, silicon, vanadium, and zinc (pp. 224-57). Washington, DC: The National Academies Press.
- Anton, S. D., Morrison, C. D., Cefalu, W. T., Martin, C. K., Coulon, S., Geiselman, P., … & Williamson, D. A. (2008). Effects of chromium picolinate on food intake and satiety. Diabetes technology & therapeutics, 10(5), 405-412.
- Tian, H., Guo, X., Wang, X., He, Z., Sun, R., Ge, S., & Zhang, Z. (2013). Chromium picolinate supplementation for overweight or obese adults.
- Onakpoya, I., Posadzki, P., & Ernst, E. (2013). Chromium supplementation in overweight and obesity: a systematic review and meta‐analysis of randomized clinical trials. obesity reviews, 14(6), 496-507.
- Gaullier, J. M., Halse, J., Høye, K., Kristiansen, K., Fagertun, H., Vik, H., & Gudmundsen, O. (2004). Conjugated linoleic acid supplementation for 1 y reduces body fat mass in healthy overweight humans. The American journal of clinical nutrition, 79(6), 1118-1125.
- Egras, A. M., Hamilton, W. R., Lenz, T. L., & Monaghan, M. S. (2010). An evidence-based review of fat modifying supplemental weight loss products. Journal of obesity, 2011.
- Lehnen, T. E., da Silva, M. R., Camacho, A., Marcadenti, A., & Lehnen, A. M. (2015). A review on effects of conjugated linoleic fatty acid (CLA) upon body composition and energetic metabolism. Journal of the International Society of Sports Nutrition, 12(1), 36.
- Onakpoya, I. J., Posadzki, P. P., Watson, L. K., Davies, L. A., & Ernst, E. (2012). The efficacy of long-term conjugated linoleic acid (CLA) supplementation on body composition in overweight and obese individuals: a systematic review and meta-analysis of randomized clinical trials. European journal of nutrition, 51(2), 127-134.
- Norris, L. E., Collene, A. L., Asp, M. L., Hsu, J. C., Liu, L. F., Richardson, J. R., … & Belury, M. A. (2009). Comparison of dietary conjugated linoleic acid with safflower oil on body composition in obese postmenopausal women with type 2 diabetes mellitus–. The American journal of clinical nutrition, 90(3), 468-476.
- Chen, S. C., Lin, Y. H., Huang, H. P., Hsu, W. L., Houng, J. Y., & Huang, C. K. (2012). Effect of conjugated linoleic acid supplementation on weight loss and body fat composition in a Chinese population. Nutrition, 28(5), 559-565.
- Ribeiro, A. S., Pina, F. L. C., Dodero, S. R., Silva, D. R., Schoenfeld, B. J., Sugihara, P., … & Tirapegui, J. (2016). Effect of conjugated linoleic acid associated with aerobic exercise on body fat and lipid profile in obese women: A randomized, double-blinded, and placebo-controlled trial. International journal of sport nutrition and exercise metabolism, 26(2), 135-144.
- Kim, J. H., Kim, Y., Kim, Y. J., & Park, Y. (2016). Conjugated linoleic acid: potential health benefits as a functional food ingredient. Annual review of food science and technology, 7, 221-244.
- Márquez, F., Babio, N., Bulló, M., & Salas-Salvadó, J. (2012). Evaluation of the safety and efficacy of hydroxycitric acid or Garcinia cambogia extracts in humans. Critical reviews in food science and nutrition, 52(7), 585-594.
- Saper, R. B., Eisenberg, D. M., & Phillips, R. S. (2004). Common dietary supplements for weight loss. American family physician, 70, 1731-1740.
- Lenz, T. L., & Hamilton, W. R. (2004). Supplemental products used for weight loss. Journal of the American Pharmacists Association, 44(1), 59-68.
- Igho, O., Kang, H. S., Rachel, P., Barbara, W., & Edzard, E. (2010). The use of Garcinia extract (hydroxycitric acid) as a weight loss supplement: a systematic review and meta-analysis of randomised clinical trials. Journal of obesity, 2011.
- Mattes, R. D., & Bormann, L. (2000). Effects of (−)-hydroxycitric acid on appetitive variables. Physiology & behavior, 71(1-2), 87-94.
- Heymsfield, S. B., Allison, D. B., Vasselli, J. R., Pietrobelli, A., Greenfield, D., & Nunez, C. (1998). Garcinia cambogia (hydroxycitric acid) as a potential antiobesity agent: a randomized controlled trial. Jama, 280(18), 1596-1600.
- Chuah, L. O., Ho, W. Y., Beh, B. K., & Yeap, S. K. (2013). Updates on antiobesity effect of garcinia origin (−)-HCA. Evidence-Based Complementary and Alternative Medicine, 2013.
- Hendrickson, B. P., Shaikh, N., Occhiogrosso, M., & Penzner, J. B. (2016). Mania induced by Garcinia cambogia: a case series. The primary care companion for CNS disorders, 18(2).
- Choi, B. K., Park, S. B., Lee, D. R., Lee, H. J., Jin, Y. Y., Yang, S. H., & Suh, J. W. (2016). Green coffee bean extract improves obesity by decreasing body fat in high-fat diet-induced obese mice. Asian Pacific journal of tropical medicine, 9(7), 635-643.
- Song, S. J., Choi, S., & Park, T. (2014). Decaffeinated green coffee bean extract attenuates diet-induced obesity and insulin resistance in mice. Evidence-Based Complementary and Alternative Medicine, 2014.
- Onakpoya, I., Terry, R., & Ernst, E. (2011). The use of green coffee extract as a weight loss supplement: a systematic review and meta-analysis of randomised clinical trials. Gastroenterology research and practice, 2011.
- Grove, K. A., & Lambert, J. D. (2010). Laboratory, epidemiological, and human intervention studies show that tea (Camellia sinensis) may be useful in the prevention of obesity. The Journal of nutrition, 140(3), 446-453.
- Hursel, R., & Westerterp-Plantenga, M. S. (2013). Catechin-and caffeine-rich teas for control of body weight in humans–. The American journal of clinical nutrition, 98(6), 1682S-1693S.
- Rains, T. M., Agarwal, S., & Maki, K. C. (2011). Antiobesity effects of green tea catechins: a mechanistic review. The Journal of nutritional biochemistry, 22(1), 1-7.
- Janssens, P. L., Hursel, R., & Westerterp-Plantenga, M. S. (2016). Nutraceuticals for body-weight management: The role of green tea catechins. Physiology & behavior, 162, 83-87.
- Türközü, D., & Tek, N. A. (2017). A minireview of effects of green tea on energy expenditure. Critical reviews in food science and nutrition, 57(2), 254-258.
- Lochocka, K., Bajerska, J., Glapa, A., Fidler-Witon, E., Nowak, J. K., Szczapa, T., … & Walkowiak, J. (2015). Green tea extract decreases starch digestion and absorption from a test meal in humans: a randomized, placebo-controlled crossover study. Scientific reports, 5, 12015.
- Jurgens, T. M., Whelan, A. M., Killian, L., Doucette, S., Kirk, S., & Foy, E. (2012). Green tea for weight loss and weight maintenance in overweight or obese adults.
- Phung, O. J., Baker, W. L., Matthews, L. J., Lanosa, M., Thorne, A., & Coleman, C. I. (2009). Effect of green tea catechins with or without caffeine on anthropometric measures: a systematic review and meta-analysis–. The American journal of clinical nutrition, 91(1), 73-81.
- Dostal, A. M., Samavat, H., Espejo, L., Arikawa, A. Y., Stendell-Hollis, N. R., & Kurzer, M. S. (2015). Green Tea Extract and Catechol-O-Methyltransferase Genotype Modify Fasting Serum Insulin and Plasma Adiponectin Concentrations in a Randomized Controlled Trial of Overweight and Obese Postmenopausal Women–. The Journal of nutrition, 146(1), 38-45.
- Hursel, R., Viechtbauer, W., & Westerterp-Plantenga, M. S. (2009). The effects of green tea on weight loss and weight maintenance: a meta-analysis. International journal of obesity, 33(9), 956.
- EFSA Panel on Dietetic Products, Nutrition and Allergies (NDA). Scientific opinion on the substantiation of health claims related to Camellia sinensis (L.) kuntze (tea), including catechins from green tea, and contribution to the maintenance or achievement of a normal body weight (ID 1107, 1112, 1544, 2716), increased beta-oxidation of fatty acids leading to a reduction in body fat mass (ID 1123, 1124, 3698), and maintenance of normal blood glucose concentrations (ID 1115, 1545) pursuant to Article 13(1) of Regulation (EC) No 1924/2006. EFSA Journal 2010;8:1791-812.
- Jurgens, T. M., Whelan, A. M., Killian, L., Doucette, S., Kirk, S., & Foy, E. (2012). Green tea for weight loss and weight maintenance in overweight or obese adults.
- National Toxicology Program, National Institutes of Health. NTP technical report on the toxicology studies of green tea extract in F344/ntac rats and B6C3F1/N mice and toxicology and carcinogenesis studies of green tea extract in Wistar Han [Crl:WI(Han)] rats and B6C3F1/N mice (gavage studies).external link disclaimer 2016.
- Yu, Z., Samavat, H., Dostal, A., Wang, R., Torkelson, C. J., Yang, C. S., … & Yuan, J. M. (2017). Effect of green tea supplements on liver enzyme elevation: results from a randomized intervention study in the United States. Cancer Prevention Research, canprevres-0160.
- Frank, J., George, T. W., Lodge, J. K., Rodriguez-Mateos, A. M., Spencer, J. P., Minihane, A. M., & Rimbach, G. (2008). Daily consumption of an aqueous green tea extract supplement does not impair liver function or alter cardiovascular disease risk biomarkers in healthy men. The Journal of Nutrition, 139(1), 58-62.
- Navarro, V. J., Khan, I., Björnsson, E., Seeff, L. B., Serrano, J., & Hoofnagle, J. H. (2017). Liver injury from herbal and dietary supplements. Hepatology, 65(1), 363-373.
- Sarma, D. N., Barrett, M. L., Chavez, M. L., Gardiner, P., Ko, R., Mahady, G. B., … & Dog, T. L. (2008). Safety of green tea extracts. Drug safety, 31(6), 469-484.
- Sender, R., Fuchs, S., & Milo, R. (2016). Revised estimates for the number of human and bacteria cells in the body. PLoS biology, 14(8), e1002533.
- Moran, C. P., & Shanahan, F. (2014). Gut microbiota and obesity: role in aetiology and potential therapeutic target. Best practice & research Clinical gastroenterology, 28(4), 585-597.
- Davis, C. D. (2016). The gut microbiome and its role in obesity. Nutrition today, 51(4), 167.
- Park, D. Y., Ahn, Y. T., Park, S. H., Huh, C. S., Yoo, S. R., Yu, R., … & Choi, M. S. (2013). Supplementation of Lactobacillus curvatus HY7601 and Lactobacillus plantarum KY1032 in diet-induced obese mice is associated with gut microbial changes and reduction in obesity. PloS one, 8(3), e59470.
- Kadooka, Y., Sato, M., Ogawa, A., Miyoshi, M., Uenishi, H., Ogawa, H., … & Tsuchida, T. (2013). Effect of Lactobacillus gasseri SBT2055 in fermented milk on abdominal adiposity in adults in a randomised controlled trial. British Journal of Nutrition, 110(9), 1696-1703.
- Park, S., & Bae, J. H. (2015). Probiotics for weight loss: a systematic review and meta-analysis. Nutrition Research, 35(7), 566-575.
- National Center for Complementary and Integrative Health, National Institutes of Health. Probiotcs: in depthexternal link disclaimer. 2017.